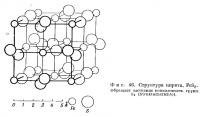
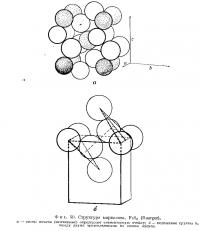
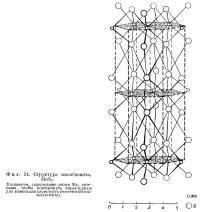
Структура пирита изображена схематично на фиг. 46. Мы можем сравнить ее со структурой NaCl, если предположим, что Fe заменяет Na, а группа S2 заменяет Cl. Гантелеобразные группы S2 ориентированы таким образом, что в каждом из восьми малых кубов, на которые разделен элементарный куб, имеется только одна группа, направленная к его центру. Тройные оси вдоль диагоналей куба, на которых лежат группы S2, не пересекаются.
Расстояние между двумя атомами серы составляет 2,10 Å. Эта величина значительно меньше удвоенного радиуса иона серы, равного 3,5 Å. Следовательно, атомы серы соединены ковалентной связью. На рисунке они сближены сильнее, чем требуется, чтобы сделать более очевидным соответствие между рассматриваемой структурой и структурой NaCl. Каждый атом серы связан с другим атомом серы и с треугольником из атомов железа. Таким образом, можно считать, что группа S2, рассматриваемая как единое целое, окружена шестью атомами металла, подобно Cl в NaCl. Каждый атом железа окружен шестью атому ми серы, причем расстояние Fe — S равно 2,26 Å.
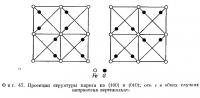
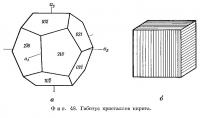
В левой части фиг. 47 изображена проекция структуры пирита на плоскость куба (100), а в правой части — проекция на плоскость (010), причем ось с в обоих случаях вертикальна. Пары атомов S, которые в первом случае параллельны оси с, во втором случае перпендикулярны ей. Симметрия кристалла гемиэдрическая, как это видно на примере кристаллов, показанных на фиг. 48. Штриховка на кубическом образце пирита имеет взаимно перпендикулярные направления на соседних гранях и обнаруживает особенности, аналогичные изображенным на проекции пирита на фиг. 47. Таким образом, структура пирита отвечает его внешней симметрии. С помощью рентгеновского анализа можно доказать, что штриховка на плоскостях куба параллельна парам атомов серы на проекциях.
К группе пирита относятся следующие минералы:

Минералы хлоантит и смальтин, состав которых иногда выражают формулами NiAs2 и CoAs2 соответственно, неправильно относят к группе пирита. Установлено, что их структуры подобны структуре скуттерудита, CoAs3, который описан на стр. 83.
Ульманит, NiSbS. Структура этого манерала очень сходна со структурой пирита, но кристаллы характеризуются самой низкой кубической симметрией (23). В ульманите никель занимает положения железа в структуре FeS2, а группы SbS — положения S2.
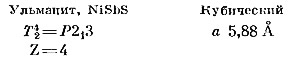
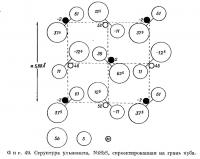
Центр симметрии, который в пирите находится посредине между атомами группы S2, в ульманите отсутствует. Структура ульманита, расшифрованная Такеути (Takeuchi, 1957), приведена на фиг. 49. Ее можно сравнить с проекцией структуры пирита на плоскость (010) (фиг. 47). Она почти соответствует структуре FeS2, однако необходимо отметить, что атомы никеля смещены по направлению тройных осей, в то время как в FeS2 атомы железа строго занимают узлы кубической гранецентрированной решетки, поскольку они лежат в центрах симметрии. Согласно Такеути, смещения атомов вдоль осей, выраженные в долях длинной диагонали куба, соответствуют следующим значениям:

Расстояние Sb — S, равное 2,40 Å, сравнимо с соответствующим расстоянием S — S в пирите, равным 2,10 Å. Атом никеля на полярной тройной оси лежит между тремя атомами Sb с одной стороны и тремя атомами серы — с другой. Расстояния Ni — Sb = 2,57 Å, Ni — S = 2,34 Å.
Кобальтин, CoAsS, и герсдорфит, NiAsS. Эти минералы обычно относили к той же группе, что и ульманит. Однако Пикок и Генри (Peacock, Henry, 1948) не смогли обнаружить дополнительных рентгеновских рефлексов, указывающих на низкую симметрию класса ульманита. Они пришли к выводу, что рассматриваемые кристаллы сходны с пиритом. По-видимому, это объясняется тем, что атомы As и S распределены беспорядочно и, следовательно, статистически эквивалентны. Такеути подчеркивает неудовлетворительное качество кристаллов этих двух минералов, так что вполне вероятно, что они еще могут оказаться аналогами ульманита.
Ниже приведены размеры элементарных ячеек кобальтина и гередорфита.
Марказит, FeS2, лёллингит, FeAs2, и раммельсбергит, NiAs2. Структуры Марказита и лёллингита расшифрованы Бюргером (Buerger, 1932). Структура кристаллов ромбическая, но в ней содержатся те же группы S2 или As2 между двумя треугольниками из атомов железа, что и в пирите. Рассматриваемые структуры изображены на фиг. 50.
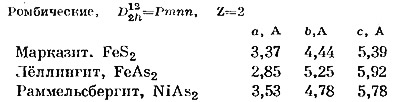
Атомы железа занимают вершины и центр ромбической ячейки.Наклонные группы S2 и As2 расположены посредине расстояния между атомами железа в направлении оси с и лежат в плоскостях симметрии. На фиг. 50, а в центре ячейки виден атом железа, окруженный шестью атомами S или As. На фиг. 50, б показаны группы S2 или As2 с треугольниками из атомов железа с обеих сторон, как в пирите.
По данным Каймена (Kaiman. 1947), раммельсбергит имеет ромбическую структуру типа марказита.
Арсенопирит, FcAsS, и гудмундит, FeSbS. Структура арсенопирита была исследована Бюргером (Buerger, 1936). Она имеет много общего со структурой марказита, и в первом приближении соотношение координации атомов в арсенопирите и в марказите, FeS2, такое же, как в ульманите и пирите. Каждый атом железа окружен несколько искаженным октаэдром, одной гранью которого является треугольник из атомов мышьяка, а другой — треугольник из атомов серы. Бюргер показал, что структура довольно сложная. Кажущиеся ромбическими кристаллы в действительности представляют собой агрегаты двойников, а истинная симметрия моноклинная и представляет собой сверхструктуру, основанную на простом расположении атомов, как в марказите. Симметрия структуры арсенопирита C52h. Если ее представить в виде Р21/с для сравнения ортогональных осей арсенопирита с аналогичными осями марказита, то размеры элементарной ячейки примут следующие значения: а 6,68, b 10,04, с 5,93 Å1).
Оси а и b удвоены по сравнению с осями структуры марказита, и элементарная ячейка содержит 8[FeAsS]. Подобную структуру имеет и гудмундит.
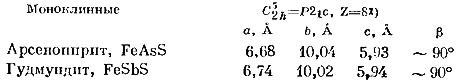
Молибденит, MoS2. «Слоистая» структура молибденита отличается от всех структур, описанных в настоящей главе. Слой атомов молибдена заключен между двумя слоями атомов серы. Эти три слоя образуют «слой» структуры, параллельный основанию гексагонального кристалла. Связь между атомами в слое довольно прочная, но сила притяжения между слоями слабая и кристаллы молибденита чрезвычайно легко расслаиваются по плоскостям спайности, подобно другим слоистым структурам. Структура изображена на фиг. 51.
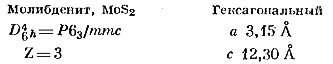
Примечания
1. х) Для такой ячейки (β ~ 90°) символ пространственной группы после перемены наименования осей (а, b, с = b', С', а') будет не Р21/с, а B21/d (Z=8). Фактически (Buerger, 1936) ячейка арсенопирита с группой P21/с имеет иные размеры: а 5,74, b 5,65, с 5,74, β 111°58', Z=4.